近日,我校生物制药研究所在中科院一区TOP期刊《JOURNAL OF AGRICULTURAL AND FOOD CHEMISTRY》上发表题为“Complex Interplay and Catalytic Versatility of Tailoring Enzymes for Efficient and Selective Biosynthesis of Fungal Mycotoxins”的研究论文(https://pubs.acs.org/doi/10.1021/acs.jafc.2c07681)。红宝石官方网站hbs16为该论文的第一单位,药学院钟永军博士为该论文的共第一作者,浙江大学毛旭明教授和陈学鹏教授为通讯作者。
真菌毒素(Mycotoxins)是农业生产和食品保藏中的一类重要污染物,是食品安全的主要威胁因子之一。真菌毒素产生菌大多天然栖息在农产品和食品上,如蘑菇内生真菌齿梗孢霉(Calcarisporium arbuscula)能产生aurovertins,生防真菌金龟子绿僵菌(Metarihzium anisopliae)和大米中的异冠裸胞壳(Emericella variecolor)能产生asteltoxin,多个已报道的青霉和曲霉菌株能产生公认食品真菌毒素citreoviridin。食品上往往同时滋生多种真菌,使得真菌毒素产生情况变得更加复杂,因为除了天然宿主的合成以外,还存在真菌间的生物转化,尤其是跨物种间的生物转化有可能显著提高真菌毒素的毒性,造成严重伤害。
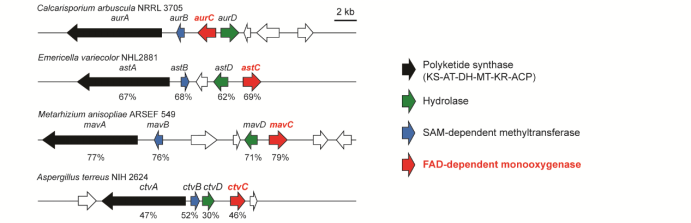
图1为吡喃酮-多烯类真菌毒素aurovertins、asteltoxin、citreoviridin生物合成基因簇
该研究利用四种真菌结构类似的吡喃酮-多烯真菌毒素aurovertins,asteltoxin 和citreoviridin生物合成基因簇为模型(图1),展示了不同来源的黄素依赖单加氧酶(FMOs)与甲基转移酶(MTs)间的复杂相互作用及其催化功能的多样性(图2)。该研究有助于利用跨物种生物合成酶高效和选择性生物合成与这些结构相关的真菌毒素,为农业和食品安全风险评估和防控真菌毒素提供理论依据。
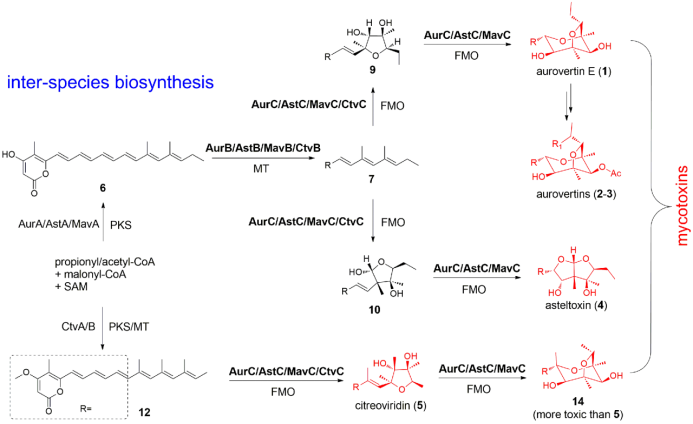
图2为不同来源FMOs与MTs间的复杂相互作用及其催化功能多样性